 Figura
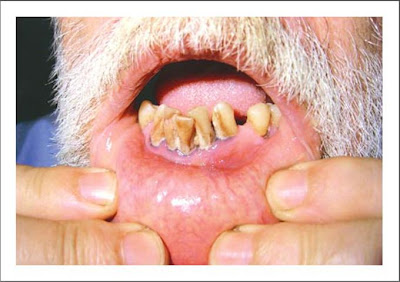
Figura: Bullas fláccidas con costras periorales sugestivas de Síndrome de la piel escaldada estafilocóccico. El paciente mejoró rápidamente su condición con tratamiento de Nafcilina
RESUMEN
Introducción
El síndrome estafilocócico de piel escaldada (SEPE), trastorno que se observa con frecuencia en lactantes y niños, es producido por una cepa particular de Staphylococcus aureus que ocasiona la formación de ampollas en la capa superior de la piel mediante la liberación de una exotoxina. Existe cierta relación entre la extensión de la enfermedad, la cantidad de exotoxina producida y el lugar de liberación de la toxina (local o sistémica). La entidad fue descrita por primera vez en 1878, y en 1970 se descubrió al agente etiológico. En 1972 se describió el primer caso en un adulto, síndrome infrecuente en esta población.
Diagnóstico
El diagnóstico del síndrome se basa en hallazgos clínicos, histológicos y microbiológicos. El paciente puede presentar hiperalgesia, eritema, descamación o formación de bullas. La evidencia histopatológica revela clivaje intraepidérmico en el estrato granuloso. Entre los hallazgos microbiológicos se encuentra el aislamiento de S. aureus productores de exotoxinas exfoliativas A o B (ETA y ETB). Por último, la ausencia de pénfigo foliáceo según la inmunofluorescencia directa o indirecta también es diagnóstica.
Características clínicas
El síndrome se observa principalmente en menores de 5 años, con un pródromo de dolor de garganta o conjuntivitis. La última puede ser intensa, con edema periorbitario y secreción purulenta. En las 48 horas posteriores el paciente presenta fiebre, malestar general y áreas eritematosas extremadamente hiperalgésicas en cara, axilas, cuello e ingles. El examen físico revela bullas laxas en las áreas eritematosas con signo de Nikolsky positivo. Las bullas son comunes en los pliegues aunque pueden extenderse a otras áreas del cuerpo. Las ampollas crecen y se rompen dejando una base eritematosa húmeda que da la apariencia de piel escaldada, cuya curación no deja cicatrices. El síndrome suele presentarse una vez y con el tratamiento adecuado resuelve en días. Sin embargo, en pacientes con formación excesiva de ampollas, principalmente adultos, el tratamiento puede verse complicado por la aparición de hipotermia, hipotensión, trastornos hidroelectrolíticos, neutropenia, distrés respiratorio e infecciones secundarias. En contraste con el SEPE, la necrólisis epidérmica tóxica (NET) se observa en casos aislados en mayores de 20 años con antecedentes de consumo de algún fármaco. Las lesiones de la NET se inician en zonas distales y comprometen las membranas mucosas. La NET es distinguible del SEPE por medio de histología convencional, con necrosis epidérmica en la primera. Por último, no existe una terapia curativa para la NET, entidad asociada con una mortalidad del 50%.
Histología
La histopatología de las erosiones revela una separación subcorneal en la capa celular granulosa debido a acantólisis intraepidérmica, con escaso infiltrado celular inflamatorio en dermis sin necrosis celular. La microscopía electrónica confirma el ensanchamiento de los espacios intracelulares en la capa granulosa, con pérdida de desmosomas. Las características histológicas de la capa granulosa son similares a las observadas en el impétigo bulloso, aunque la entidad presenta un pronunciado infiltrado inflamatorio. Por otra parte, la NET cursa con necrosis celular epidérmica y degeneración vacuolar de la capa basal, que puede producir una separación dermoepidérmica. El grosor del techo epidérmico permite la diferenciación histológica rápida de las dos entidades.
Microbiología
El síndrome se produce en sujetos con infección oculta o manifiesta por S. aureus productor de exotoxina exfoliativa o en individuos colonizados por el germen. La mayoría de los patógenos aislados pertenecen al grupo fagos II subtipos 3A, 3B, 3C, 55 y 71. Con menor frecuencia, el síndrome es producido S. aureus grupos I y III. La secreción de exotoxinas se produce durante la fase de crecimiento bacteriano. Las mismas exotoxinas inducen la formación de lesiones localizadas en el impétigo bulloso, producidas por inoculación directa, mientras que en el SEPE las lesiones son el producto de la circulación sistémica de la toxina. La ETA es producida por el 89% de los patógenos aislados. En la mayoría de los casos, la tipificación del S. aureus productor de exotoxinas es suficiente para el diagnóstico de SEPE. Entre los métodos para la detección de exotoxinas exfoliativas se encuentran la inmunodifusión doble, hemaglutinación, radioinmunoensayo, enzimoinmunoensayo e hibridación del ADN. La reacción en cadena de la polimerasa ofrece mayor precisión diagnóstica. En los niños, la transmisión del patógeno puede producirse mediante portadores asintomáticos, fenómeno que destaca la importancia de su pesquisa.
Por otra parte, el microorganismo generalmente es aislado en la mayoría de los adultos y en menos del 3% de los casos pediátricos.
Aproximadamente el 5% de las cepas de S. aureus cultivadas en el hospital producen exotoxinas exfoliativas. La colonización con patógenos productores de exotoxinas exfoliativas es mayor en los neonatos, con un 3% de portadores asintomáticos. Por otra parte, un estudio reveló que el 1% de las gestantes evaluadas eran portadoras asintomáticas. Sin embargo, a pesar de las elevadas tasas de colonización, el SEPE es infrecuente, destacan los autores.
Patogénesis
La toxina exfoliativa posee gran especificidad para producir la pérdida de la adhesión celular mediada por desmosomas sólo en la epidermis superficial. Estudios inmunohistoquímicos revelaron que la ETA se une a la filagrina en los gránulos de queratohialina de las células de la capa granulosa. Debido a que la filagrina constituye el anclaje intracelular de los desmosomas, esto condujo a la hipótesis de que la separación intradérmica es consecuencia de la ruptura de los desmosomas por la actividad proteolítica de la toxina. La desmogleína I, importante proteína de los desmosomas, sería el blanco de las exotoxinas exfoliativas. Otra teoría indica que las 2 toxinas exfoliativas actuarían como superantígenos, aunque la falta de infiltrado inflamatorio no sustenta esta noción. A pesar de la elevada prevalencia de S. aureus productor de ETA y ETB es probable que intervengan otros factores en la patogenia del síndrome. El SEPE no es común en los adultos sanos, probablemente debido a la formación de anticuerpos contra ETA y ETB, que comprometería el efecto de las toxinas. De hecho, el 91% de los adultos presenta anticuerpos contra ETA. En contraste, sólo el 30% de los individuos con edades comprendidas entre los 3 meses y los 2 años evidencia anticuerpos antiETA, valor que asciende al 42% entre los 2 y los 5 años.
Factores predisponentes
La producción excesiva de endotoxina, el incremento de la tasa de portadores de S. aureus y el aumento de la susceptibilidad a la toxina son fundamentales en la producción del SEPE. La insuficiencia renal es el cofactor más frecuente en adultos con SEPE, mientras que la proliferación excesiva de S. aureus ocupa el segundo lugar.
Tratamiento
El diagnóstico rápido y el tratamiento temprano con antibióticos antiestafilocócicos por vía parenteral, como flucloxacilina, es esencial. Todas las cepas de S. aureus aisladas son resistentes a la penicilina y sensibles a penicilinas semisintéticas. Las ampollas deben permanecer intactas, mientras que es conveniente cubrir las áreas erosionadas con gasas impregnadas en vaselina blanca. La conjuntivitis puede ser tratada con antibióticos tópicos o ungüentos antisépticos. Por otra parte, los pacientes con grandes extensiones de la piel afectadas requieren la internación en unidades de cuidados intensivos, colchones especiales, tratamiento del dolor, regulación de la temperatura, hidratación, sostén nutricional, evaluación del riesgo de infección y cuidados dermatológicos. Los corticoides están contraindicados en el tratamiento del SEPE debido a que empeoran el cuadro.
Por otra parte, debe considerarse la pesquisa de portadores ante el diagnóstico simultáneo de varios casos. Los portadores deben suspender el cuidado de niños menores de 2 años y ser tratados con una penicilina semisintética resistente a betalactamasas.
Pronóstico
La mortalidad en los niños asciende al 4%, asociada con compromiso cutáneo importante, sepsis y desequilibrio hidroelectrolítico. Sin embargo, la mortalidad en el adulto puede superar el 60%, fenómeno asociado en gran medida a los factores subyacentes irreversibles que predisponen al síndrome.
Conclusiones
El SEPE posee una presentación clínica característica en los niños que facilita su diagnóstico temprano y el tratamiento adecuado. La terapia es sencilla cuando el cuadro es leve y en ausencia de patologías asociadas, aunque puede ser más compleja en pacientes particularmente enfermos. Finalmente, los autores destacan que la entidad todavía está asociada con mortalidad, especialmente entre los adultos.
Bibliografía:
NEJM Image Challenge
American Journal of Clinical Dermatology 4(3):165-175, 2003
 de Enfermedad de Paget ósea con compromiso en pelvis de 7 años de evolución que comienza con dolor en región lumbar izquierda y sacro con irradiación radicular que no calma con analgésicos comunes. Se solicita una TAC de sacro y columna lumbar que muestra compromiso sacro por la osteopatía previamente diagnosticada a lo que se asocia una masa de partes blandas en pelvis menor que compromete el agujero obturador izquierdo.
de Enfermedad de Paget ósea con compromiso en pelvis de 7 años de evolución que comienza con dolor en región lumbar izquierda y sacro con irradiación radicular que no calma con analgésicos comunes. Se solicita una TAC de sacro y columna lumbar que muestra compromiso sacro por la osteopatía previamente diagnosticada a lo que se asocia una masa de partes blandas en pelvis menor que compromete el agujero obturador izquierdo. tesis diagnóstica sea en este momento la mas aceptada en la sala.
tesis diagnóstica sea en este momento la mas aceptada en la sala. de la masa pelviana
de la masa pelviana
































 ateneo pareció no estar relacionada podría tener alguna relación con la enfermedad de base del paciente
ateneo pareció no estar relacionada podría tener alguna relación con la enfermedad de base del paciente nico), o después de 6 meses (osteosarcoma metacrónico). Sin embargo el osteosarcoma multifocal es una entidad rara y se ve en menores de 10 años.
nico), o después de 6 meses (osteosarcoma metacrónico). Sin embargo el osteosarcoma multifocal es una entidad rara y se ve en menores de 10 años.




