Una mujer de 35 años, diestra, con antecedentes de infección por VIH fue internada en un hospital por presentar cefalea y alteración de su estado mental después de un accidente automovilístico.
Más temprano, el día de la internación, mientras conducía su vehículo sin cinturón de seguridad, sufrió una colisión contra otro vehículo a baja velocidad, recibiendo traumatismo de cráneo. En ningún momento perdió la conciencia, pero los testigos que presenciaron el accidente, y los que la acompañaron al hospital, dijeron que la paciente actuaba en forma extraña. En la evaluación en el hospital, se objetivó que la paciente estaba desorientada. No había signos de trauma, y los signos vitales eran normales. Los resultados de los exámenes de laboratorio de rutina eran normales. Una TAC de cráneo sin administración de sustancia de contraste reveló áreas prominentes de baja atenuación en ambos hemisferios, sin contusiones hemorrágicas. Se le administró dexametasona intravenosa y fue derivada a otro hospital de mayor complejidad.
En el departamento de emergencias del otro hospital, la paciente refirió cefalea de leve intensidad pero ningún otro síntoma. No recordaba el accidente.
Cuatro años antes se le había realizado un diagnóstico de infección por VIH después de una consulta ginecológica donde se le encontró una displasia cervical de alto grado. El recuento de linfocitos T CD4 fue en ese momento de 211/mm3, y la carga viral RNA VIH fue de 476.000 copias/ml. No había evidencias de coinfección activa con hepatitis B ni C, sífilis, o Mycobacterium tuberculosis. Anticuerpos anticitomegalovirus (CMV) fueron detectados en el suero de la paciente; en cambio, no se detectaron anticuerpos contra Toxoplasma gondii.
Se comenzó tratamiento antirretroviral; subsecuentemente el recuento de CD4 permaneció consistentemente por encima de 200 células/mm3, y la carga viral de RNA VIH cayó a menos de 400 copias/ml.
Dos años antes de la actual internación, comenzó con episodios de cefalea diarias, los cuales fueron empeorando gradualmente. La paciente en ese momento consultó al hospital donde se le realizó una punción lumbar; el líquido reveló un aumento de la celularidad a predominio linfocitario. Fue tratada con aciclovir intravenoso, y las cefaleas se fueron resolviendo en un período de dos meses.
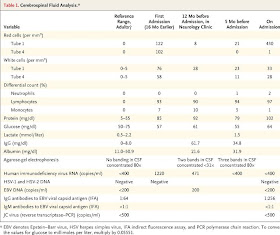
Seis meses más tarde, comenzó nuevamente con episodios de cefalea todos los días. Fue internada nuevamente por cefalea severa con malestar general, fotofobia, vómitos, e inestabilidad en la marcha. La RMN de cerebro después de la administración de gadolinio reveló realce leptomeningeo difuso con hiperintensidades asimétricas extensas en T2 y FLAIR en la sustancia blanca profunda de los hemisferios cerebrales, ganglios basales, y región dorsal de la protuberancia. Los anticuerpos IgG contra herpes simplex tipo 2 (HSV-2) eran positivos en el suero; los resultados del estudio del líquido cefalorraquídeo se muestran en la Tabla 1.
Tabla 1.
Análisis del Líquido Cefalorraquídeo.
Se hizo diagnóstico de meningitis de Mollaret (meningitis aséptica recurrente causada generalmente por virus de la familia Herpesviridae), y se comenzó nuevamente con aciclovir en forma intravenosa por 10 días. La paciente fue dada de alta después de los 10 días de tratamiento parenteral, con valaciclovir por vía oral y seguimiento por consultorio de neurología.
Cuando la paciente fue vista por neurología un año antes de la actual internación, la cefalea había mejorado algo y no refería otros síntomas. La paciente describía la cefalea como sorda, leve, constante, generalizada, y no presentaba signos de foco. El examen del fondo de ojo mostraba edema de papila bilateral. El examen neurológico incluyó una evaluación cognitiva básica que fue normal.
Dos semanas más tarde una punción lumbar mostró una presión de apertura de38 cm de agua. Los resultados de los tests de laboratorio se muestran en la Tabla 1 y Tabla 2.
Tabla 2.
Resultado de los Exámenes Hematológicos y Séricos.
Se le administró acetazolamida pero la paciente no la tomó.
Un mes más tarde, en una consulta de seguimiento, la cefalea había mejorado y el edema de papila se había resuelto. Los resultados del líquido cefalorraquídeo llevados a cabo cuando la paciente estaba asintomática se muestran en la Tabla 1.
La RMN de seguimiento cuando la paciente estaba asintomática reveló resolución del realce paquimeníngeo pero persistencia de las anormalidades de señal en la sustancia blanca de ambos hemisferios. Durante los meses siguientes ella se sintió bien excepto por recurrencia breve de cefalea asociada a trastornos de memoria 5 meses antes de la internación, que se resolvieron espontáneamente.
Los antecedentes de la paciente incluian neumonía bacteriana, depresión leve, y una histerectomía llevada a cabo debido a displasia cervical.
En la internación, su medicación incluia lopinavir asociado con ritonavir, emtricitabina, tenofovir, valaciclovir, y paroxetina.
La paciente no tenía alergias conocidas a medicamentos.
Había nacido en África sub-Sahariana y había emigrado a los EE UU 6 años antes. Estaba divorciada y trabajaba como enfermera. No tenía hijos. Tomaba alcohol ocasionalmente. No fumaba ni usaba drogas ilícitas. Había tenido cinco compañeros sexuales en toda su vida, pero actualmente no tenía una vida sexualmente activa. Una hermana había muerto de SIDA en África. Sus padres y otros hermanos estaban sanos. No tenía antecedentes de enfermedades neurológicas.
En el examen la paciente estaba alerta pero sorprendida y atemorizada, orientada, pero con limitada comprensión de la situación. Estaba desatenta y fácilmente distraible, e incapaz de articular frases coherentemente. Su nivel de actividad variaba desde retardo psicomotor severo hasta la agitación. Seguía las órdenes, pero era incapaz de realizar actividades más complejas. Su lenguaje parecía normal, aunque hablaba poco. Los tests de otras esferas cognitivas estaban alterados por la falta de atención. Los signos vitales eran normales. Las pupilas eran asimétricas, de3 mm de diámetro, y levemente reactivas a la luz. Los reflejos osteotendinosos estaban vivos, y la respuesta plantar era extensora bilateralmente. El resto del examen neurológico era normal.
Una RMN de cráneo después de la administración de gadolinio reveló extensa anormalidad en la señal dentro de la sustancia blanca, en una distribución diferente a la observada en un reciente estudio de 4 meses antes, con áreas de mejoramiento pero con compromiso de nuevas áreas. El realce meníngeo no era evidente. La angio-RMN de cabeza y cuello era normal.
La paciente fue admitida al servicio de neurología donde continuó con su medicación habitual. Se notó incontinencia urinaria el primer día de internación. El segundo día, se realizó una punción lumbar, y el líquido mostró una presión de apertura de20 cm de agua. Los resultados del LCR se muestran en la Tabla 1.
Un electroencefalograma mostró ondas tetha difusas lentas, con ondas delta más prominentes.
El sexto día se llevó a cabo un procedimiento diagnóstico.
Diagnóstico Diferencial.
Cuatro años antes de la internación actual, esta mujer de 35 años fue diagnostica de infección por VIH y comenzó tratamiento antirretroviral sin complicaciones. Después de la iniciación de la terapia antirretroviral su recuento de CD4 permaneció en forma estable por encima de 200 células/mm3 y su nivel de carga viral RNA-VIH, por debajo de 400 copias de RNA/ml. Esta buena respuesta a la terapia es crítica cuando se formulan diagnósticos diferenciales, ya que muchas de las clásicas complicaciones neurológicas asociadas a VIH-SIDA, ocurren generalmente cuando el recuento de linfocitos CD4 caen por debajo de 200 células/mm3. Un año antes de la internación actual, la paciente fue evaluada en un servicio de neurología, por discretos episodios de meningoencefalitis, asociadas a imágenes neurológicas marcadamente anormales en cerebro. Es importante notar que la linfocitosis en LCR y las alteraciones en las imágenes, persistieron aún después de la completa recuperación clínica.
Imágenes de Cerebro.
Una RMN de cerebro fue llevada a cabo durante el episodio inicial de meningitis aséptica. Las imágenes en T1 obtenidas después de la administración de material de contraste fue remarcable por el intenso realce leptomeníngeo. Lesiones de anormalidades de señal, hiperintensas multifocales fueron vistas en T2 y FLAIR (Figura 1A), y afectaban todas las zonas del cerebro, incluyendo la sustancia blanca subcortical profunda de los hemisferios cerebrales, ganglios de la base, y región dorsal de la protuberancia.
Figura 1. Estudio de Imágenes de Cerebro.
Imágenes obtenidas con fluid-attenuated inversion recovery (FLAIR), la RMN inicial de cerebro revela anormalidades de señal, hiperintensas que afectan la sustancia blanca subcortical profunda y a nivel de los ventrículos laterales (Panel A). Las imágenes con FLAIR llevadas a cabo 2 años más tarde, en el momento de la internación, muestran una significativa progresión de las alteraciones de la señal (Panel B). Las imágenes con FLAIR obtenidas 1 año antes de la iniciación del tratamiento con corticoides revela lesiones multifocales de hiperintensidades en la señal (Panel C); sin embargo, las alteraciones son menos extensas que las vistas en imágenes previas.
Las alteraciones de señal con hiperintensidades en T2 persistieron pero con cambios sutiles en las RMN de los 2 años siguientes. La RMN de cerebro 2 años después del examen inicial, en el momento del deterioro severo en la condición de la paciente (Figura 1B), no reveló realce leptomeníngeo ni paquimeníngeo, pero reveló progresión de las alteraciones de señal de la sustancia blanca, con compromiso más extenso del cerebro y especialmente en fosa posterior. Las imágenes mostraron variaciones regionales en la alteración de la señal T2. Además, había estrechamiento de los ventrículos y los surcos, indicativos de edema difuso.
Cuál es el Diagnóstico?
Discusión.
La presentación clínica remitente recidivante, junto a alteraciones persistentes del líquido cefalorraquídeo y de las imágenes, son inusuales en el contexto de un paciente con infección por VIH bien controlada. Los episodios subagudos de cefalea, aumento de la celularidad, realce transitorio difuso de las leptomeninges, edema de papila, y elevación de la presión de apertura en la punción lumbar se deben más probablemente a meningoencefalitis crónica con empeoramientos intermitentes. Las alteraciones de las imágenes son inusuales dado lo extenso de las mismas, el compromiso dinámico de la sustancia blanca, y el compromiso progresivo del tronco cerebral. La presencia de bandas oligoclonales, y la producción de IgG intratecal en la electroforesis del LCR, sugieren que la enfermedad es inflamatoria.
Durante mucho tiempo en esta paciente (dos años), existió una marcada disparidad entre lo extenso de las alteraciones observadas en las imágenes, y el grado de deterioro clínico, lo que es sugestivo de que la enfermedad no conduce a destrucción irreversible del tejido, tal como se ve en infecciones fulminantes, vasculitis, o neoplasias.
El deterioro brusco en la condición clínica de la paciente después de un accidente automovilístico menor, recuerda las dramáticas descompensaciones descriptas en algunas leucoencefalopatías.
Meningoencefalitis Crónicas con Alteraciones de la Sustancia Blanca.
En resumen, esta paciente, con infección por VIH bien controlada se presentó con compromiso extenso de la sustancia blanca, el cual implica una muy amplia lista de diagnósticos diferenciales. (Tabla 3)
Tabla 3. Diagnóstico Diferencial de las Enfermedades de la Sustancia Blanca en pacientes con Infección por VIH.
En la Tabla, CADASIL son las siglas de cerebral autosomal dominant arteriopathy with subcortical infarcts and leukoencephalopathy.
En la Tabla, marcadas con una +: Condiciones que pueden cursar con meningoencefalitis crónica.
En la Tabla, neuro ISIS (Immune Reconstitution Inflammatory Syndrome), se refiere las manifestaciones neurológicas del síndrome de recostitución inmune.
El reconocimiento de una meningoencefalitis crónica ayuda a estrechar el diagnóstico diferencial, ya que hay un número limitado de condiciones en las que esas dos condiciones ocurren juntas.
Ciertos diagnósticos, aunque improbables, deben ser mencionados. La leucoencefelopatía multifocal progresiva (LMP), ocurre muy raramente cuando el recuento de linfocitos T-CD4 excede las 200 células/mm3. La LMP no se asocia a linfocitosis en el LCR, y la ausencia de DNA del virus JC en el LCR (1) hace que este diagnóstico sea muy improbable. En forma similar, las enfermedades relacionadas al virus de Epstein-Barr (EBV) (por ejemplo meningoencefalitis y linfoma primario de SNC), son improbables, debido a que esos trastornos raramente ocurren en pacientes con recuentos periféricos de linfocitos T-CD4 mayores de 100 células/mm3. En una ocasión se detectaron 200 copias de EBV/ml en el LCR de esta paciente. Una muestra de LCR posterior, mostró 2100 copias /ml de EBV, sugiriendo un “escape” del virus al compartimiento del LCR. Sin embargo, los tests de ácidos nucleicos para EBV realizados con posterioridad, incluyendo el llevado a cabo en la última internación, fueron negativos. Una reactivación leve de EBV sin síntomas no es infrecuente en pacientes con VIH, y no tiene consecuencias particulares (2).
Las leucoencefalopatías tóxicas son improbables en este caso, dado el aumento de la celularidad en el LCR y a la ausencia de exposición conocida a sustancias tóxicas para la sustancia blanca.
Las enfermedades desmielinizantes han sido reportadas en pacientes con infección con VIH.
Enfermedades similares a la encefalomielitis diseminada aguda pueden ocurrir en pacientes con seroconversión VIH, particularmente en niños (3). La encefalomielitis diseminada aguda es improbable en este caso, ya que existe un gran espacio de tiempo entre la seroconversión y el primer síntoma clínico; además, aunque la encefalomielitis diseminada aguda es un síndrome monofásico, la historia de esta paciente es prolongada.
La desmielinización multifocal similar a la vista en casos de esclerosis múltiple, ha sido reportada en pacientes con infección por VIH. Sin embargo, tanto la meningoencefalitis, como las alteraciones en las imágenes vistas en esta paciente son atípicas para esclerosis múltiple. Las meningoencefalitis causadas por Herpesviridae, particularmente HSV-1 y HSV-2, tienden a ser monofásicas, a menudo severas, y que no se asocian a alteraciones crónicas del LCR.
La meningitis de Mollaret se caracteriza por episodios recurrentes de cefalea severa, meningismo, fiebre, y aumento de la celularidad en el LCR, con remisiones espontáneas que duran semanas a meses; ahora se cree que es causada por el HSV en la mayoría de los casos. En esta paciente, la PCR en LCR para DNA-HSV fue negativo en tres ocasiones, haciendo improbable el diagnóstico de meningitis de Mollaret.
La meningoencefalitis aguda es un cuadro conocido en el síndrome de seroconversión agudo por VIH, pero ha sido reportado también en pacientes con infección crónica por VIH, típicamente aquellos que tienen elevadas cargas virales de VIH en el LCR, (4) las cuales no existían en esta paciente. En forma similar, un síndrome del compartimiento intratecal por VIH (persistencia de la replicación VIH en SNC, a pesar de supresión virológica en sangre) es improbable en vista de las bien controladas cargas virales plasmáticas y mínimos niveles de RNA-VIH en LCR.
Trastornos Neurocognitivos Asociados a VIH.
La infección por VIH se asocia a un espectro de síndromes de disfunción cognitiva, que están agrupados bajo el nombre de: trastornos neurocognitivos asociados a VIH (5). Esos síndromes van desde un trastorno neurocognitivo asintomático, detectado sólo por teswts dirigidos a desenmascararlos, pasando por un leve trastorno neurocognitivo sintomático, hasta la demencia asociada a VIH. Alguna de estas formas de compromiso neurocognitivo se ve en40 a 60% de las personas infectadas con VIH, reflejando su neurovirulencia. Estos términos clínicos se acompañan de un espectro de anormalidades neuropatológicas directamente relacionadas a la infección del parénquima cerebral por el VIH, o a la activación inmune inducida por el VIH, o a ambas. Los pacientes que son tratados con antirretrovirales en forma efectiva están protegidos de la demencia asociada al VIH, pero, la terapia antirretroviral no parece prevenir los trastornos asintomáticos o los trastornos neurocognitivos leves, (6) que son probablemente debidos a injuria morfológicamente más sutil de las sinapsis y las dendritas (7,8). Este tipo de injurias son particularmente evidentes en el cuerpo estriado, en el hipocampo, y la corteza prefrontal, y se correlacionan clínicamente con las alteraciones del pensamiento abstracto, la flexibilidad mental, la atención, el juicio, y la velocidad psicomotora.
Esta paciente tenía alteraciones importantes del LCR y alteraciones en las imágenes. Los pacientes con trastornos neurocognitivos activos asociados a VIH no tienen alteraciones, o sólo alteraciones leves del LCR, y sólo los pacientes con demencia asociada a VIH tienen evidencias de alteraciones de la sustancia blanca en las imágenes. Además, los trastornos asintomáticos, o los trastornos neurocognitivos leves pueden ocurrir en pacientes con infección VIH bien controlada, pero la demencia asociada al VIH es una manifestación avanzada infección VIH no tratada. En esta paciente, un trastorno neurocognitivos asociados a VIH parece improbable ya que la infección por VIH estaba bien controlada, y, tanto el LCR como las imágenes no son típicas de ningún subtipo de trastornos neurocognitivos asociados a VIH.
Leucoencefalopatía asociada a VIH.
Las alteraciones del la sustancia blanca vistas en esta paciente evocan el diagnóstico de leucoencefalopatía asociada a VIH, un síndrome descripto en pacientes que tienen infección avanzada con virus VIH, niveles marcadamente elevados de RNA-VIH en plasma y LCR, y compromiso inmune clínicamente significativo (9). La leucoencefalopatía asociada a VIH se caracteriza por una profunda demencia subcortical, con compromiso difuso marcado y confluente de la sustancia blanca en las imágenes. Este síndrome es probablemente una forma fulminante de demencia asociada a VIH, y una forma de encefalitis que afecta la sustancia blanca en particular. A pesar de las alteraciones difusas de la sustancia blanca en esta paciente, la infección sistémica VIH estaba controlada.
Sindrome de Reconstitución Inmune (SRI).
El síndrome de reconstitución inmune (immune reconstitution inflammatory syndrome) (IRIS) fue reportado por primera vez en 1992. Es una apropiada pero excesiva respuesta inmune a un estímulo antigénico, generalmente de naturaleza infecciosa, en el contexto de la recuperación inmune, después de la iniciación de terapia antirretroviral (10,11). Después de la iniciación de la terapia antirretroviral, los niveles plasmáticos de RNA-VIH caen típicamente a menos de 10% de los niveles pre-terapéuticos al cabo de dos semanas. Paralelamente, ocurre un aumento bifásico en el recuento de linfocitos T CD4, asociado a un moderado aumento del recuento de los linfocitos T CD8. Cuando este proceso de reconstitución inmune ocurre en presencia de un estímulo antigénico (sea un antígeno extraño como un autoantígeno), la reacción inmune al antígeno puede ser excesiva y patológica, conduciendo en este caso al SRI.
Aunque una coinfección (sirviendo como estímulo antigénico extraño) puede ser conocida (y aún ya tratada) en el momento de la iniciación de la terapia antirretroviral, una infección latente es a menudo desenmascarada por la respuesta inmune recargada. Una amplia variedad de agentes infecciosos han estado implicados en el SRI sistémico, particularmente M. tuberculosis, otras mycobacterias, y CMV. El SRI puede conducir a otros síndromes no infecciosos inmunomediados tales como la enfermedad de Graves (12), y la sarcoidosis (13). Hasta donde sabemos, esta paciente no tenía otras coinfecciones, aunque debido a que es oriunda del África sub Sahariana, su riesgo de albergar una infección latente como por ejemplo tuberculosis, está aumentado.
El SRI sistémico es usualmente leve y autolimitado, y la mayoría de los casos ocurren dentro de los 3 meses después de la iniciación de la terapia antirretroviral. La enfermedad de esta paciente comenzó 2 años después de la iniciación de la terapia antirretroviral, y pareció estar limitada al sistema nervioso central.
La presentación neurológica del SRI (neuro-SRI) parece mucho menos común que el SRI sistémico con una incidencia estimada de menos de 1% (14,15). Como el SRI sistémico, los casos de neuro-SRI con infecciones coexistentes han sido descriptos. La infección más común es el virus JC, causa de la leucoencefalopatía multifocal progresiva (LMP) (15,16), y la infección por Cryptococcus neoformans (16). Recientes reportes enfatizan que la terapia antirrretroviral puede haber sido comenzada antes de que la LMP se haya reconocido, llevando a una confusión diagnóstica y a una notable morbimortalidad (5 a 15%) a pesar del tratamiento (14,15). Menos frecuentemente, el SRI ocurre con coinfección con T. gondii, CMV, varicella–zoster virus, HSV, or parvovirus B19 (17-21). Un dato de extrema importancia es, que muchos pacientes con neuro-SRI pueden no mostrar evidencias de coinfección (14,16,22,23). En tales casos, el estímulo antigénico de base puede ser dado por componentes del VIH en si mismo, o autoantígenos. Alternativamente, un escape ocasional de VIH u otros virus (por ej EBV) a través de la barrera hematoencefálica pueden servir como provocadores antigénicos. Si nuestra paciente tenía neuro-SRI, uno de esos dos escenarios serían la explicación más probable.
Alteraciones difusas en el estudio con imágenes, similares a las vistas en esta paciente, han sido descriptas en neuro-SRI sin evidencia de coinfección (14,16). En forma similar, el aumento de los linfocitos en el LCR ha sido reportado (14).
Para realizar un diagnóstico definitivo de neuro-SRI, y descartar definitivamente otros diagnósticos, fueron llevados a cabo una biopsia abierta del lóbulo frontal y de las meninges .
Diagnóstico Presuntivo:
Síndrome de reconstitución inmune neurológico (neuro-SRI).
Discusión Patológica:
La biopsia del lóbulo frontal derecho incluia leptomeninges, corteza cerebral, y sustancia blanca subyacente. Las leptomeninges eran finas y delicadas sin evidencias de infiltrados inflamatorios. La corteza estaba apropiadamente poblada por neuronas, con laminación intacta. No había evidencias de encefalitis, ya que la corteza carecía de nódulos microgliales, neurofagia, o gliosis reactiva. Había vasos esparcidos por la corteza cerebral con importantes infiltrados celulares inflamatorios perivasculares, y aún más vasos en la sustancia blanca subcortical con dichos infiltrados (Figura 2A)
Figura 2. Biopsia de Cerebro.
Una biopsia de lóbulo frontal fue llevada a cabo. La toma de la corteza muestra arquitectura normal, e infiltrados perivasculares multifocales pero no celularidad leptomeningea (Panel A hematoxilina-eosina). El infiltrado perivascular está compuesto por pequeñas células inflamatorias, sin evidencia de injuria de la pared vascular (Panel B hematoxilina-eosina).
La tinción inmunohistoquímica para CD3 muestra que e infiltrado consiste en células T, con extensión del infiltrado linfocitario al parénquima (Panel C), y la mayoría de las células T expresan CD8 (Panel D).
Las células inflamatorias son una mezcla de poblaciones constituidas por linfocitos, macrófagos, y ocasionales células plasmáticas (Figura 2B), a diferencia de la población monofásica de pequeños linfocitos que son características de las cencefalitis virales o las células atípicas del linfoma de sistema nervioso central. No existe injuria de la pared de los vasos, como se ve en las vasculitis.
Además de los infiltrados de células inflamatorias, la sustancia blanca estaba bien preservada, sin pérdida de mielina. No había hallazgos anatomopatológicos de encefalopatía por VIH, caracterizados clásicamente por infiltrados macrofágicos o células mononucleares con células multinucleadas (sincitios) tanto en la sustancia gris como en la sustancia blanca. El análisis inmunohistoquímico para antígenos de VIH (gp41) fue negativo. Tinciones especiales para organismos, incluyendo espiroquetas fueron negativos. No había tampoco hallazgos histológicos compatibles con LMP (oligodendrocitos agrandados con cromatina de aspecto cristalino y grandes astrocitos con marcado pleomorfismo nuclear). Además, el análisis inmunohistoquímico para análisis de antígenos de virus JC fue negativo.
El análisis inmunohistoquímico reveló que los infiltrados de células inflamatorias estaba compuesto predominantemente por células CD3 y CD8 (Figura2C ), acompañados por macrófagos CD68 dispersos; no había células CD20. Células CD3 y CD8 estaban también aumentados en número en la sustancia blanca, alejados de los vasos sanguíneos (Figura 2D). Todos estos hallazgos son consistentes con SRI de cerebro.
Los hallazgos histológicos del compromiso de cerebro por SIR (neuro-SRI) habían sido definidos en estos últimos años como fenómenos que acompañan a la terapia antirretroviral (23,24). Aunque este síndrome es más comúnmente visto en pacientes con infecciones oportunistas de cerebro (16,25), puede también ser observado en ausencia de tal estímulo. En pacientes sin tales estímulos, la respuesta puede estar dirigida contra autoantígenos, o contra antígenos asociados a VIH (23). No encontramos evidencias de infección en esta paciente, lo cual es sugestivo que el mecanismo patogénico en este caso es la segunda causa (respuesta inmune dirigida contra antígenos asociados a VIH), aunque la ausencia de evidencia de otra infección está siempre limitada por la sensibilidad de los métodos de detección.
Manejo y Seguimiento.
El status mental de la paciente mejoró espontáneamente, y fue dada de alta a un centro de rehabilitación el día 12º de su internación, y retornó a su hogar 9 días más tarde.
En una visita de seguimiento 3 días más tarde, la paciente estaba en su estado normal basal. Dado que ya sus síntomas habían desaparecido y vuelto a aparecer en otras oportunidades, dado también que la biopsia había arrojado neuro-SRI, y dado que se descartó infección oportunista, se comenzó con 60 mg de prednisona diarios, debido a las alteraciones en las imágenes y al riesgo de ulterior deterioro en la condición de la paciente. La terapia antirretroviral no se cambió.
La paciente fue monitoreada clínicamente y con RMN seriadas. La dosis de prednisona se fue bajando en un año hasta llegar a 5 mg por día, y se suspendió definitivamente después de 2,5 años, momento en el cual las alteraciones de la sustancia blanca se habían casi resuelto (Figura1C ). La paciente está actualmente trabajando en tiempo completo. Sus déficits cognitivos están casi completamente resueltos, y sus cefaleas no han reaparecido; está siendo tratada por depresión leve.
Este caso nos recuerda que las formas crónicas de SRI existen, a veces con un largo intervalo entre la iniciación de la terapia antirretroviral y el desarrollo de los síntomas (24 meses en esta paciente). Ella tuvo una dramática y sostenida respuesta clínica a los corticoides, reafirmando que el neuro-SRI es potencialmente tratable si es reconocido.
Una RMN llevada a cabo después del tratamiento, reveló alteraciones multifocales de hiperintensidad en T2 y FLAIR mucho menos extensas que las imágenes iniciales
En una ocasión, hubo un bajo nivel de RNA VIH detectados en LCR, a pesar de una carga viral indetectable en plasma. Es posible que el virus hubiese persistido en SNC dado la insuficiente penetración de la terapia antirretroviral, y que todo este fenómeno sea expresión de respuesta inmune dirigida selectivamente al SNC, pero, en esta paciente, los repetidos tests confirmaron un bajo número de copias RNA VIH en el LCR. Además, las tinciones inmunohistoquímicas para gp41 fueron negativas en la biopsia cerebral. Sin embargo, es posible que un escape intermitente de VIH o EBV pueden haber servido como estímulo antigénico intermitente, lo que dio el cuadro clínico de una meningoencefalitis intermitente.
Diagnóstico Anatómico:
Síndrome de reconstitución inmune neurológico (neuro-SRI) sin evidencias de infección oportunista.
Fuente
Departments of Neurology (D.J.C.), Radiology (R.G.G.), and Pathology (M.P.F.),Massachusetts General Hospital ; and the Departments of Neurology (D.J.C.), Radiology (R.G.G.), and Pathology (M.P.F.), Harvard Medical School — both in Boston
Conclusiones del Caso.
Referencias Bibliográficas.
Más temprano, el día de la internación, mientras conducía su vehículo sin cinturón de seguridad, sufrió una colisión contra otro vehículo a baja velocidad, recibiendo traumatismo de cráneo. En ningún momento perdió la conciencia, pero los testigos que presenciaron el accidente, y los que la acompañaron al hospital, dijeron que la paciente actuaba en forma extraña. En la evaluación en el hospital, se objetivó que la paciente estaba desorientada. No había signos de trauma, y los signos vitales eran normales. Los resultados de los exámenes de laboratorio de rutina eran normales. Una TAC de cráneo sin administración de sustancia de contraste reveló áreas prominentes de baja atenuación en ambos hemisferios, sin contusiones hemorrágicas. Se le administró dexametasona intravenosa y fue derivada a otro hospital de mayor complejidad.
En el departamento de emergencias del otro hospital, la paciente refirió cefalea de leve intensidad pero ningún otro síntoma. No recordaba el accidente.
Cuatro años antes se le había realizado un diagnóstico de infección por VIH después de una consulta ginecológica donde se le encontró una displasia cervical de alto grado. El recuento de linfocitos T CD4 fue en ese momento de 211/mm3, y la carga viral RNA VIH fue de 476.000 copias/ml. No había evidencias de coinfección activa con hepatitis B ni C, sífilis, o Mycobacterium tuberculosis. Anticuerpos anticitomegalovirus (CMV) fueron detectados en el suero de la paciente; en cambio, no se detectaron anticuerpos contra Toxoplasma gondii.
Se comenzó tratamiento antirretroviral; subsecuentemente el recuento de CD4 permaneció consistentemente por encima de 200 células/mm3, y la carga viral de RNA VIH cayó a menos de 400 copias/ml.
Dos años antes de la actual internación, comenzó con episodios de cefalea diarias, los cuales fueron empeorando gradualmente. La paciente en ese momento consultó al hospital donde se le realizó una punción lumbar; el líquido reveló un aumento de la celularidad a predominio linfocitario. Fue tratada con aciclovir intravenoso, y las cefaleas se fueron resolviendo en un período de dos meses.
Seis meses más tarde, comenzó nuevamente con episodios de cefalea todos los días. Fue internada nuevamente por cefalea severa con malestar general, fotofobia, vómitos, e inestabilidad en la marcha. La RMN de cerebro después de la administración de gadolinio reveló realce leptomeningeo difuso con hiperintensidades asimétricas extensas en T2 y FLAIR en la sustancia blanca profunda de los hemisferios cerebrales, ganglios basales, y región dorsal de la protuberancia. Los anticuerpos IgG contra herpes simplex tipo 2 (HSV-2) eran positivos en el suero; los resultados del estudio del líquido cefalorraquídeo se muestran en la Tabla 1.
Tabla 1.
Análisis del Líquido Cefalorraquídeo.
Se hizo diagnóstico de meningitis de Mollaret (meningitis aséptica recurrente causada generalmente por virus de la familia Herpesviridae), y se comenzó nuevamente con aciclovir en forma intravenosa por 10 días. La paciente fue dada de alta después de los 10 días de tratamiento parenteral, con valaciclovir por vía oral y seguimiento por consultorio de neurología.
Cuando la paciente fue vista por neurología un año antes de la actual internación, la cefalea había mejorado algo y no refería otros síntomas. La paciente describía la cefalea como sorda, leve, constante, generalizada, y no presentaba signos de foco. El examen del fondo de ojo mostraba edema de papila bilateral. El examen neurológico incluyó una evaluación cognitiva básica que fue normal.
Dos semanas más tarde una punción lumbar mostró una presión de apertura de
Tabla 2.
Resultado de los Exámenes Hematológicos y Séricos.
Se le administró acetazolamida pero la paciente no la tomó.
Un mes más tarde, en una consulta de seguimiento, la cefalea había mejorado y el edema de papila se había resuelto. Los resultados del líquido cefalorraquídeo llevados a cabo cuando la paciente estaba asintomática se muestran en la Tabla 1.
La RMN de seguimiento cuando la paciente estaba asintomática reveló resolución del realce paquimeníngeo pero persistencia de las anormalidades de señal en la sustancia blanca de ambos hemisferios. Durante los meses siguientes ella se sintió bien excepto por recurrencia breve de cefalea asociada a trastornos de memoria 5 meses antes de la internación, que se resolvieron espontáneamente.
Los antecedentes de la paciente incluian neumonía bacteriana, depresión leve, y una histerectomía llevada a cabo debido a displasia cervical.
En la internación, su medicación incluia lopinavir asociado con ritonavir, emtricitabina, tenofovir, valaciclovir, y paroxetina.
La paciente no tenía alergias conocidas a medicamentos.
Había nacido en África sub-Sahariana y había emigrado a los EE UU 6 años antes. Estaba divorciada y trabajaba como enfermera. No tenía hijos. Tomaba alcohol ocasionalmente. No fumaba ni usaba drogas ilícitas. Había tenido cinco compañeros sexuales en toda su vida, pero actualmente no tenía una vida sexualmente activa. Una hermana había muerto de SIDA en África. Sus padres y otros hermanos estaban sanos. No tenía antecedentes de enfermedades neurológicas.
En el examen la paciente estaba alerta pero sorprendida y atemorizada, orientada, pero con limitada comprensión de la situación. Estaba desatenta y fácilmente distraible, e incapaz de articular frases coherentemente. Su nivel de actividad variaba desde retardo psicomotor severo hasta la agitación. Seguía las órdenes, pero era incapaz de realizar actividades más complejas. Su lenguaje parecía normal, aunque hablaba poco. Los tests de otras esferas cognitivas estaban alterados por la falta de atención. Los signos vitales eran normales. Las pupilas eran asimétricas, de
Una RMN de cráneo después de la administración de gadolinio reveló extensa anormalidad en la señal dentro de la sustancia blanca, en una distribución diferente a la observada en un reciente estudio de 4 meses antes, con áreas de mejoramiento pero con compromiso de nuevas áreas. El realce meníngeo no era evidente. La angio-RMN de cabeza y cuello era normal.
La paciente fue admitida al servicio de neurología donde continuó con su medicación habitual. Se notó incontinencia urinaria el primer día de internación. El segundo día, se realizó una punción lumbar, y el líquido mostró una presión de apertura de
Un electroencefalograma mostró ondas tetha difusas lentas, con ondas delta más prominentes.
El sexto día se llevó a cabo un procedimiento diagnóstico.
Diagnóstico Diferencial.
Cuatro años antes de la internación actual, esta mujer de 35 años fue diagnostica de infección por VIH y comenzó tratamiento antirretroviral sin complicaciones. Después de la iniciación de la terapia antirretroviral su recuento de CD4 permaneció en forma estable por encima de 200 células/mm3 y su nivel de carga viral RNA-VIH, por debajo de 400 copias de RNA/ml. Esta buena respuesta a la terapia es crítica cuando se formulan diagnósticos diferenciales, ya que muchas de las clásicas complicaciones neurológicas asociadas a VIH-SIDA, ocurren generalmente cuando el recuento de linfocitos CD4 caen por debajo de 200 células/mm3. Un año antes de la internación actual, la paciente fue evaluada en un servicio de neurología, por discretos episodios de meningoencefalitis, asociadas a imágenes neurológicas marcadamente anormales en cerebro. Es importante notar que la linfocitosis en LCR y las alteraciones en las imágenes, persistieron aún después de la completa recuperación clínica.
Imágenes de Cerebro.
Una RMN de cerebro fue llevada a cabo durante el episodio inicial de meningitis aséptica. Las imágenes en T1 obtenidas después de la administración de material de contraste fue remarcable por el intenso realce leptomeníngeo. Lesiones de anormalidades de señal, hiperintensas multifocales fueron vistas en T2 y FLAIR (Figura 1A), y afectaban todas las zonas del cerebro, incluyendo la sustancia blanca subcortical profunda de los hemisferios cerebrales, ganglios de la base, y región dorsal de la protuberancia.
Figura 1. Estudio de Imágenes de Cerebro.
Imágenes obtenidas con fluid-attenuated inversion recovery (FLAIR), la RMN inicial de cerebro revela anormalidades de señal, hiperintensas que afectan la sustancia blanca subcortical profunda y a nivel de los ventrículos laterales (Panel A). Las imágenes con FLAIR llevadas a cabo 2 años más tarde, en el momento de la internación, muestran una significativa progresión de las alteraciones de la señal (Panel B). Las imágenes con FLAIR obtenidas 1 año antes de la iniciación del tratamiento con corticoides revela lesiones multifocales de hiperintensidades en la señal (Panel C); sin embargo, las alteraciones son menos extensas que las vistas en imágenes previas.
Las alteraciones de señal con hiperintensidades en T2 persistieron pero con cambios sutiles en las RMN de los 2 años siguientes. La RMN de cerebro 2 años después del examen inicial, en el momento del deterioro severo en la condición de la paciente (Figura 1B), no reveló realce leptomeníngeo ni paquimeníngeo, pero reveló progresión de las alteraciones de señal de la sustancia blanca, con compromiso más extenso del cerebro y especialmente en fosa posterior. Las imágenes mostraron variaciones regionales en la alteración de la señal T2. Además, había estrechamiento de los ventrículos y los surcos, indicativos de edema difuso.
Cuál es el Diagnóstico?
Discusión.
La presentación clínica remitente recidivante, junto a alteraciones persistentes del líquido cefalorraquídeo y de las imágenes, son inusuales en el contexto de un paciente con infección por VIH bien controlada. Los episodios subagudos de cefalea, aumento de la celularidad, realce transitorio difuso de las leptomeninges, edema de papila, y elevación de la presión de apertura en la punción lumbar se deben más probablemente a meningoencefalitis crónica con empeoramientos intermitentes. Las alteraciones de las imágenes son inusuales dado lo extenso de las mismas, el compromiso dinámico de la sustancia blanca, y el compromiso progresivo del tronco cerebral. La presencia de bandas oligoclonales, y la producción de IgG intratecal en la electroforesis del LCR, sugieren que la enfermedad es inflamatoria.
Durante mucho tiempo en esta paciente (dos años), existió una marcada disparidad entre lo extenso de las alteraciones observadas en las imágenes, y el grado de deterioro clínico, lo que es sugestivo de que la enfermedad no conduce a destrucción irreversible del tejido, tal como se ve en infecciones fulminantes, vasculitis, o neoplasias.
El deterioro brusco en la condición clínica de la paciente después de un accidente automovilístico menor, recuerda las dramáticas descompensaciones descriptas en algunas leucoencefalopatías.
Meningoencefalitis Crónicas con Alteraciones de la Sustancia Blanca.
En resumen, esta paciente, con infección por VIH bien controlada se presentó con compromiso extenso de la sustancia blanca, el cual implica una muy amplia lista de diagnósticos diferenciales. (Tabla 3)
Tabla 3. Diagnóstico Diferencial de las Enfermedades de la Sustancia Blanca en pacientes con Infección por VIH.
En la Tabla, CADASIL son las siglas de cerebral autosomal dominant arteriopathy with subcortical infarcts and leukoencephalopathy.
En la Tabla, marcadas con una +: Condiciones que pueden cursar con meningoencefalitis crónica.
En la Tabla, neuro ISIS (Immune Reconstitution Inflammatory Syndrome), se refiere las manifestaciones neurológicas del síndrome de recostitución inmune.
El reconocimiento de una meningoencefalitis crónica ayuda a estrechar el diagnóstico diferencial, ya que hay un número limitado de condiciones en las que esas dos condiciones ocurren juntas.
Ciertos diagnósticos, aunque improbables, deben ser mencionados. La leucoencefelopatía multifocal progresiva (LMP), ocurre muy raramente cuando el recuento de linfocitos T-CD4 excede las 200 células/mm3. La LMP no se asocia a linfocitosis en el LCR, y la ausencia de DNA del virus JC en el LCR (1) hace que este diagnóstico sea muy improbable. En forma similar, las enfermedades relacionadas al virus de Epstein-Barr (EBV) (por ejemplo meningoencefalitis y linfoma primario de SNC), son improbables, debido a que esos trastornos raramente ocurren en pacientes con recuentos periféricos de linfocitos T-CD4 mayores de 100 células/mm3. En una ocasión se detectaron 200 copias de EBV/ml en el LCR de esta paciente. Una muestra de LCR posterior, mostró 2100 copias /ml de EBV, sugiriendo un “escape” del virus al compartimiento del LCR. Sin embargo, los tests de ácidos nucleicos para EBV realizados con posterioridad, incluyendo el llevado a cabo en la última internación, fueron negativos. Una reactivación leve de EBV sin síntomas no es infrecuente en pacientes con VIH, y no tiene consecuencias particulares (2).
Las leucoencefalopatías tóxicas son improbables en este caso, dado el aumento de la celularidad en el LCR y a la ausencia de exposición conocida a sustancias tóxicas para la sustancia blanca.
Las enfermedades desmielinizantes han sido reportadas en pacientes con infección con VIH.
Enfermedades similares a la encefalomielitis diseminada aguda pueden ocurrir en pacientes con seroconversión VIH, particularmente en niños (3). La encefalomielitis diseminada aguda es improbable en este caso, ya que existe un gran espacio de tiempo entre la seroconversión y el primer síntoma clínico; además, aunque la encefalomielitis diseminada aguda es un síndrome monofásico, la historia de esta paciente es prolongada.
La desmielinización multifocal similar a la vista en casos de esclerosis múltiple, ha sido reportada en pacientes con infección por VIH. Sin embargo, tanto la meningoencefalitis, como las alteraciones en las imágenes vistas en esta paciente son atípicas para esclerosis múltiple. Las meningoencefalitis causadas por Herpesviridae, particularmente HSV-1 y HSV-2, tienden a ser monofásicas, a menudo severas, y que no se asocian a alteraciones crónicas del LCR.
La meningitis de Mollaret se caracteriza por episodios recurrentes de cefalea severa, meningismo, fiebre, y aumento de la celularidad en el LCR, con remisiones espontáneas que duran semanas a meses; ahora se cree que es causada por el HSV en la mayoría de los casos. En esta paciente, la PCR en LCR para DNA-HSV fue negativo en tres ocasiones, haciendo improbable el diagnóstico de meningitis de Mollaret.
La meningoencefalitis aguda es un cuadro conocido en el síndrome de seroconversión agudo por VIH, pero ha sido reportado también en pacientes con infección crónica por VIH, típicamente aquellos que tienen elevadas cargas virales de VIH en el LCR, (4) las cuales no existían en esta paciente. En forma similar, un síndrome del compartimiento intratecal por VIH (persistencia de la replicación VIH en SNC, a pesar de supresión virológica en sangre) es improbable en vista de las bien controladas cargas virales plasmáticas y mínimos niveles de RNA-VIH en LCR.
Trastornos Neurocognitivos Asociados a VIH.
La infección por VIH se asocia a un espectro de síndromes de disfunción cognitiva, que están agrupados bajo el nombre de: trastornos neurocognitivos asociados a VIH (5). Esos síndromes van desde un trastorno neurocognitivo asintomático, detectado sólo por teswts dirigidos a desenmascararlos, pasando por un leve trastorno neurocognitivo sintomático, hasta la demencia asociada a VIH. Alguna de estas formas de compromiso neurocognitivo se ve en
Esta paciente tenía alteraciones importantes del LCR y alteraciones en las imágenes. Los pacientes con trastornos neurocognitivos activos asociados a VIH no tienen alteraciones, o sólo alteraciones leves del LCR, y sólo los pacientes con demencia asociada a VIH tienen evidencias de alteraciones de la sustancia blanca en las imágenes. Además, los trastornos asintomáticos, o los trastornos neurocognitivos leves pueden ocurrir en pacientes con infección VIH bien controlada, pero la demencia asociada al VIH es una manifestación avanzada infección VIH no tratada. En esta paciente, un trastorno neurocognitivos asociados a VIH parece improbable ya que la infección por VIH estaba bien controlada, y, tanto el LCR como las imágenes no son típicas de ningún subtipo de trastornos neurocognitivos asociados a VIH.
Leucoencefalopatía asociada a VIH.
Las alteraciones del la sustancia blanca vistas en esta paciente evocan el diagnóstico de leucoencefalopatía asociada a VIH, un síndrome descripto en pacientes que tienen infección avanzada con virus VIH, niveles marcadamente elevados de RNA-VIH en plasma y LCR, y compromiso inmune clínicamente significativo (9). La leucoencefalopatía asociada a VIH se caracteriza por una profunda demencia subcortical, con compromiso difuso marcado y confluente de la sustancia blanca en las imágenes. Este síndrome es probablemente una forma fulminante de demencia asociada a VIH, y una forma de encefalitis que afecta la sustancia blanca en particular. A pesar de las alteraciones difusas de la sustancia blanca en esta paciente, la infección sistémica VIH estaba controlada.
Sindrome de Reconstitución Inmune (SRI).
El síndrome de reconstitución inmune (immune reconstitution inflammatory syndrome) (IRIS) fue reportado por primera vez en 1992. Es una apropiada pero excesiva respuesta inmune a un estímulo antigénico, generalmente de naturaleza infecciosa, en el contexto de la recuperación inmune, después de la iniciación de terapia antirretroviral (10,11). Después de la iniciación de la terapia antirretroviral, los niveles plasmáticos de RNA-VIH caen típicamente a menos de 10% de los niveles pre-terapéuticos al cabo de dos semanas. Paralelamente, ocurre un aumento bifásico en el recuento de linfocitos T CD4, asociado a un moderado aumento del recuento de los linfocitos T CD8. Cuando este proceso de reconstitución inmune ocurre en presencia de un estímulo antigénico (sea un antígeno extraño como un autoantígeno), la reacción inmune al antígeno puede ser excesiva y patológica, conduciendo en este caso al SRI.
Aunque una coinfección (sirviendo como estímulo antigénico extraño) puede ser conocida (y aún ya tratada) en el momento de la iniciación de la terapia antirretroviral, una infección latente es a menudo desenmascarada por la respuesta inmune recargada. Una amplia variedad de agentes infecciosos han estado implicados en el SRI sistémico, particularmente M. tuberculosis, otras mycobacterias, y CMV. El SRI puede conducir a otros síndromes no infecciosos inmunomediados tales como la enfermedad de Graves (12), y la sarcoidosis (13). Hasta donde sabemos, esta paciente no tenía otras coinfecciones, aunque debido a que es oriunda del África sub Sahariana, su riesgo de albergar una infección latente como por ejemplo tuberculosis, está aumentado.
El SRI sistémico es usualmente leve y autolimitado, y la mayoría de los casos ocurren dentro de los 3 meses después de la iniciación de la terapia antirretroviral. La enfermedad de esta paciente comenzó 2 años después de la iniciación de la terapia antirretroviral, y pareció estar limitada al sistema nervioso central.
La presentación neurológica del SRI (neuro-SRI) parece mucho menos común que el SRI sistémico con una incidencia estimada de menos de 1% (14,15). Como el SRI sistémico, los casos de neuro-SRI con infecciones coexistentes han sido descriptos. La infección más común es el virus JC, causa de la leucoencefalopatía multifocal progresiva (LMP) (15,16), y la infección por Cryptococcus neoformans (16). Recientes reportes enfatizan que la terapia antirrretroviral puede haber sido comenzada antes de que la LMP se haya reconocido, llevando a una confusión diagnóstica y a una notable morbimortalidad (
Alteraciones difusas en el estudio con imágenes, similares a las vistas en esta paciente, han sido descriptas en neuro-SRI sin evidencia de coinfección (14,16). En forma similar, el aumento de los linfocitos en el LCR ha sido reportado (14).
Para realizar un diagnóstico definitivo de neuro-SRI, y descartar definitivamente otros diagnósticos, fueron llevados a cabo una biopsia abierta del lóbulo frontal y de las meninges .
Diagnóstico Presuntivo:
Síndrome de reconstitución inmune neurológico (neuro-SRI).
Discusión Patológica:
La biopsia del lóbulo frontal derecho incluia leptomeninges, corteza cerebral, y sustancia blanca subyacente. Las leptomeninges eran finas y delicadas sin evidencias de infiltrados inflamatorios. La corteza estaba apropiadamente poblada por neuronas, con laminación intacta. No había evidencias de encefalitis, ya que la corteza carecía de nódulos microgliales, neurofagia, o gliosis reactiva. Había vasos esparcidos por la corteza cerebral con importantes infiltrados celulares inflamatorios perivasculares, y aún más vasos en la sustancia blanca subcortical con dichos infiltrados (Figura 2A)
Figura 2. Biopsia de Cerebro.
Una biopsia de lóbulo frontal fue llevada a cabo. La toma de la corteza muestra arquitectura normal, e infiltrados perivasculares multifocales pero no celularidad leptomeningea (Panel A hematoxilina-eosina). El infiltrado perivascular está compuesto por pequeñas células inflamatorias, sin evidencia de injuria de la pared vascular (Panel B hematoxilina-eosina).
La tinción inmunohistoquímica para CD3 muestra que e infiltrado consiste en células T, con extensión del infiltrado linfocitario al parénquima (Panel C), y la mayoría de las células T expresan CD8 (Panel D).
Las células inflamatorias son una mezcla de poblaciones constituidas por linfocitos, macrófagos, y ocasionales células plasmáticas (Figura 2B), a diferencia de la población monofásica de pequeños linfocitos que son características de las cencefalitis virales o las células atípicas del linfoma de sistema nervioso central. No existe injuria de la pared de los vasos, como se ve en las vasculitis.
Además de los infiltrados de células inflamatorias, la sustancia blanca estaba bien preservada, sin pérdida de mielina. No había hallazgos anatomopatológicos de encefalopatía por VIH, caracterizados clásicamente por infiltrados macrofágicos o células mononucleares con células multinucleadas (sincitios) tanto en la sustancia gris como en la sustancia blanca. El análisis inmunohistoquímico para antígenos de VIH (gp41) fue negativo. Tinciones especiales para organismos, incluyendo espiroquetas fueron negativos. No había tampoco hallazgos histológicos compatibles con LMP (oligodendrocitos agrandados con cromatina de aspecto cristalino y grandes astrocitos con marcado pleomorfismo nuclear). Además, el análisis inmunohistoquímico para análisis de antígenos de virus JC fue negativo.
El análisis inmunohistoquímico reveló que los infiltrados de células inflamatorias estaba compuesto predominantemente por células CD3 y CD8 (Figura
Los hallazgos histológicos del compromiso de cerebro por SIR (neuro-SRI) habían sido definidos en estos últimos años como fenómenos que acompañan a la terapia antirretroviral (23,24). Aunque este síndrome es más comúnmente visto en pacientes con infecciones oportunistas de cerebro (16,25), puede también ser observado en ausencia de tal estímulo. En pacientes sin tales estímulos, la respuesta puede estar dirigida contra autoantígenos, o contra antígenos asociados a VIH (23). No encontramos evidencias de infección en esta paciente, lo cual es sugestivo que el mecanismo patogénico en este caso es la segunda causa (respuesta inmune dirigida contra antígenos asociados a VIH), aunque la ausencia de evidencia de otra infección está siempre limitada por la sensibilidad de los métodos de detección.
Manejo y Seguimiento.
El status mental de la paciente mejoró espontáneamente, y fue dada de alta a un centro de rehabilitación el día 12º de su internación, y retornó a su hogar 9 días más tarde.
En una visita de seguimiento 3 días más tarde, la paciente estaba en su estado normal basal. Dado que ya sus síntomas habían desaparecido y vuelto a aparecer en otras oportunidades, dado también que la biopsia había arrojado neuro-SRI, y dado que se descartó infección oportunista, se comenzó con 60 mg de prednisona diarios, debido a las alteraciones en las imágenes y al riesgo de ulterior deterioro en la condición de la paciente. La terapia antirretroviral no se cambió.
La paciente fue monitoreada clínicamente y con RMN seriadas. La dosis de prednisona se fue bajando en un año hasta llegar a 5 mg por día, y se suspendió definitivamente después de 2,5 años, momento en el cual las alteraciones de la sustancia blanca se habían casi resuelto (Figura
Este caso nos recuerda que las formas crónicas de SRI existen, a veces con un largo intervalo entre la iniciación de la terapia antirretroviral y el desarrollo de los síntomas (24 meses en esta paciente). Ella tuvo una dramática y sostenida respuesta clínica a los corticoides, reafirmando que el neuro-SRI es potencialmente tratable si es reconocido.
Una RMN llevada a cabo después del tratamiento, reveló alteraciones multifocales de hiperintensidad en T2 y FLAIR mucho menos extensas que las imágenes iniciales
En una ocasión, hubo un bajo nivel de RNA VIH detectados en LCR, a pesar de una carga viral indetectable en plasma. Es posible que el virus hubiese persistido en SNC dado la insuficiente penetración de la terapia antirretroviral, y que todo este fenómeno sea expresión de respuesta inmune dirigida selectivamente al SNC, pero, en esta paciente, los repetidos tests confirmaron un bajo número de copias RNA VIH en el LCR. Además, las tinciones inmunohistoquímicas para gp41 fueron negativas en la biopsia cerebral. Sin embargo, es posible que un escape intermitente de VIH o EBV pueden haber servido como estímulo antigénico intermitente, lo que dio el cuadro clínico de una meningoencefalitis intermitente.
Diagnóstico Anatómico:
Síndrome de reconstitución inmune neurológico (neuro-SRI) sin evidencias de infección oportunista.
Fuente
Departments of Neurology (D.J.C.), Radiology (R.G.G.), and Pathology (M.P.F.),
Conclusiones del Caso.
Esta mujer de 35 años, VIH positiva diagnosticada cuatro años antes de la actual internación, y en tratamiento antirretroviral desde entonces, comenzó su enfermedad dos años después del inicio del tratamiento, momento en el cual tenía un status inmunológico aceptable, y no habiendo presentado antes, ninguna sintomatología relacionada, aún cuando su condición inmune había estado antes, más comprometida.
La sintomatología consistía en cuadros de meningoencefalitis linfocitarias a líquido claro de comportamiento remitente-recidivante, asociado a alteraciones cognitivas leves, y con alteraciones en las imágenes cerebrales, las cuales mostraban compromiso difuso de la sustancia blanca de dos años de evolución. Se hizo un diagnóstico presuntivo de meningitis de Mollaret, a pesar de ausencia de fiebre en los episodios, de que la investigación de HSV 1 y 2 en LCR fue negativa, de la ausencia de las células características del síndrome, y de las anormalidades en las imágenes cerebrales, las cuales exceden el diagnóstico de meningitis de Mollaret.
Los episodios de cefalea eran periódicos, y seguramente en su génesis intervenían la meningoencefalitis crónica recidivante, con pleocitosis mononuclear y eritrocitos en LCR, así como una hipertensión endocraneana, evidenciada por edema de papila bilateral objetivado por lo menos en una ocasión, con aumento en la presión de apertura.
El síndrome de reconstitución inmune (SRI) planteado como explicación abarcativa del cuadro, se fundamentó en una meningoencefalitis crónica recidivante y remitente en forma espontánea, que apareció de la mano de la recuperación inmune de la paciente, asociado a un intensa respuesta humoral de anticuerpos intratecales, evidenciado por aumento de la IgG en forma de bandas oligoclonales, y habiendo descartado otras causas, especialmente las infecciosas y neoplásicas. No pudo arribarse al diagnóstico de la causa del síndrome de reconstitución inmune, si bien se especuló sobre antígenos propios del virus VIH como desencadenante de la exagerada respuesta de anticuerpos, o bien autoantígenos cerebrales normales, que por alguna razón, en el contexto de la recuperación inmune, son reconocidos como ajenos por el sistema propio de vigilancia. Estos antígenos sin embargo, no fueron encontrados en la biopsia de cerebro ni en el LCR de la paciente.
La espectacular respuesta terapéutica a la prednisona, confirma el diagnóstico de SRI.
En la próxima entrada, revisaremos el síndrome de reconstitución inmune.
Referencias Bibliográficas.
1)Koralnik IJ, Boden D, Mai VX, Lord CI, Letvin NL. JC virus DNA load in patients with and without progressive multifocal leukoencephalopathy. Neurology 1999;52:253-260
Web of Science | Medline
Web of Science | Medline
2) Plentz A, Jilg W, Kochanowski B, Ibach B, Knoll A. Detection of herpesvirus DNA in cerebrospinal fluid and correlation with clinical symptoms. Infection 2008;36:158-162
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
3) Silver B, McAvoy K, Mikesell S, Smith TW. Fulminating encephalopathy with perivenular demyelination and vacuolar myelopathy as the initial presentation of human immunodeficiency virus infection. Arch Neurol 1997;54:647-650
Web of Science | Medline
Web of Science | Medline
4) Wendel KA, McArthur JC. Acute meningoencephalitis in chronic human immunodeficiency virus (HIV) infection: putative central nervous system escape of HIV replication. Clin Infect Dis 2003;37:1107-1111
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
5) Antinori A, Arendt G, Becker JT, et al. Updated research nosology for HIV-associated neurocognitive disorders. Neurology 2007;69:1789-1799
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
6) Cysique LA, Brew BJ. Neuropsychological functioning and antiretroviral treatment in HIV/AIDS: a review. Neuropsychol Rev 2009;19:169-185
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
7) Everall IP, Heaton RK, Marcotte TD, et al. Cortical synaptic density is reduced in mild to moderate human immunodeficiency virus neurocognitive disorder. Brain Pathol 1999;9:209-217
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
8) Masliah E, Heaton RK, Marcotte TD, et al. Dendritic injury is a pathological substrate for human immunodeficiency virus-related cognitive disorders. Ann Neurol 1997;42:963-972
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
9) Langford TD, Letendre SL, Marcotte TD, et al. Severe, demyelinating leukoencephalopathy in AIDS patients on antiretroviral therapy. AIDS 2002;16:1019-1029
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
10) French MA. HIV/AIDS: immune reconstitution inflammatory syndrome: a reappraisal. Clin Infect Dis 2009;48:101-107
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
11) French MA, Mallal SA, Dawkins RL. Zidovudine-induced restoration of cell-mediated immunity to mycobacteria in immunodeficient HIV-infected patients. AIDS 1992;6:1293-1297
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
12) Crum NF Johns ST
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
13) Foulon G, Wislez M, Naccache JM, et al. Sarcoidosis in HIV-infected patients in the era of highly active antiretroviral therapy. Clin Infect Dis 2004;38:418-425
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
14) McCombe JA, Auer RN, Maingat FG, Houston S, Gill MJ, Power C. Neurologic immune reconstitution inflammatory syndrome in HIV/AIDS: outcome and epidemiology. Neurology 2009;72:835-841
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
15) Tan K, Roda R, Ostrow L, McArthur J, Nath A. PML-IRIS in patients with HIV infection: clinical manifestations and treatment with steroids. Neurology 2009;72:1458-1464
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
16) Venkataramana A, Pardo CA, McArthur JC, et al. Immune reconstitution inflammatory syndrome in the CNS of HIV-infected patients. Neurology 2006;67:383-388
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
17) Pfeffer G, Prout A, Hooge J, Maguire J. Biopsy-proven immune reconstitution syndrome in a patient with AIDS and cerebral toxoplasmosis. Neurology 2009;73:321-322
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
18) Tremont-Lukats IW, Garciarena P, Juarbe R, El-Abassi RN. The immune inflammatory reconstitution syndrome and central nervous system toxoplasmosis. Ann Intern Med 2009;150:656-657
Web of Science | Medline
Web of Science | Medline
19) Janowicz DM, Johnson RM, Gupta SK. Successful treatment of CMV ventriculitis immune reconstitution syndrome. J Neurol Neurosurg Psychiatry 2005;76:891-892
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
20) Newsome SD
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
21) Intalapaporn P, Poovorawan Y, Suankratay C. Immune reconstitution syndrome associated with parvovirus B19-induced pure red cell aplasia during highly active antiretroviral therapy. J Infect 2006;53:e79-e82
CrossRef | Medline
CrossRef | Medline
22) Gray F, Bazille C, Adle-Biassette H, Mikol J, Moulignier A, Scaravilli F. Central nervous system immune reconstitution disease in acquired immunodeficiency syndrome patients receiving highly active antiretroviral treatment. J Neurovirol 2005;11:Suppl 3:16-22
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
23) Miller RF, Isaacson PG, Hall-Craggs M, et al. Cerebral CD8+ lymphocytosis in HIV-1 infected patients with immune restoration induced by HAART. Acta Neuropathol (Berl) 2004;108:17-23
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
24) Rushing EJ, Liappis A, Smirniotopoulos JD, et al. Immune reconstitution inflammatory syndrome of the brain: case illustrations of a challenging entity. J Neuropathol Exp Neurol 2008;67:819-827
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline
25) Johnson T, Nath A. Neurological complications of immune reconstitution in HIV-infected populations. Ann N Y Acad Sci 2010;1184:106-120
CrossRef | Web of Science | Medline
CrossRef | Web of Science | Medline




Pienso que puede tratarse de una leucoencefalopatia multifocal progresiva.
ResponderEliminarEl caso presentado merece el comentario siguiente:
ResponderEliminar1- Mujer de 35 años – blanca o negra? – que inicia un proceso con los antecedentes y características evolutivas siguientes:
a) Se inició luego de un accidente automovilístico ¿ El accidente fue casual o debido a la presencia ya de trastornos cognoscitivos? Es cierto no tenía puesto el cinturón . ¿negligencia o distracción patológica?
b) Desde hacía cuatro años era HIV + en tratamiento. Dos años antes ya venía padeciendo cefaleas diarias
c) Aparentemente, y a pesar del tratamiento antirretroviral , empeora y tiene un episodio compatible con síndrome meníngeo y trastornos de la marcha – sugiere compromiso de la fosa posterior - ¿Efecto paradójico? ¿Síndrome de reconstitución inmune?
CONTINÚA.
Lo expresado hasta aquí hace pensar que la enferma pudo haber tenido el accidente automovilístico no debido a una una alteración cognoscitiva previa por ej.: olvidar colocarse el cinturón de seguridad.
ResponderEliminar2 - A pesar de no existir antecedentes de enfermedad neurológica febril de iniciación y evolución agudas, existió infección por virus herpéticos: CMV, Herpes simple-2 (sometida a histerectomía por grave displasia cervical!) , Epstein Barr (presencia de anticuerpos para capside y DNA activo en líquido cefalorraquídeo). Sabemos que las infecciones por virus herpéticos son habituales en la población humana desde el nacimiento y que alojadas en el organismo pueden reemerger como graves enfermedades oportunistas.
3- Con buen criterio se sometió a la enferma a tratamiento con acyclovir y velacyclovir bajo la lógica sospecha de que el cuadro neurológico y las imágenes existentes en la RMN eran compatibles con la hoy aceptada meningitis subaguda linfocitaria de Mollaret. Más aún, prueba del acierto presuntivo fue la evidente mejoría de la enferma y también la evolución posterior con sus altibajos típicos de las infecciones herpéticas.
CONTINÚA.
4-La observación de las imágenes situadas en el SNC revelan compromiso multifocal con evidente afectación de la substancia blanca subcortical, periventricular, de los hemisferios cerebrales, además de los ganglios de la base y la protuberancia. Asociando estas imágenes con la enfermedad marcadora y las infecciones herpéticas acontecidas en un terreno inmunocomprometido cabe presumir que estamos frente a una enfermedad desmielinizante del SNC. Sabemos que entre las etiologías virales posibles deben considerarse: virus Herpes simples, Epstein Barr, HTL-V1, Herpes tipo 6, Citomegalovirus.
ResponderEliminar5-Vinculada con la infección por VIH existe otra encefalopatía desmielinizante: la leucoencefalopatía desmielinizante multifocal progresiva, provocada por el virus JC. Sabemos que la infección por este patógeno es común y que más del 85% de la población adulta del mundo ya ha sido infectada.
Conforme a las posibilidades del huésped susceptible también este virus puede transformarse en causante de grave y mortal enfermedad neurológica, sobre todo en sujetos con infección por VIH con una caída de sus CD4 a menos de 100. Sin embargo últimas referencias bibliográficas mencionan reemergencias neurológicas con este virus aún con recuentos de CD4 de 500.
CONTINÚA.
6- Cabe ahora preguntarse: Si estamos en presencia de una enfermedad desmielinizante del SNC, cuál o cuáles pueden ser sus etiologías?
ResponderEliminarLa enferma, que sin duda padeció una exacerbación sistémica de su infección herpética en los comienzos de su infección por HIV, con bajos CD4 (211/mm3) y carga viral de 476.000 copias/ml ), pudo bien iniciar un padecimiento del SNC por estos virus– de ahí su mejoría parcial al tratarla con acyclovir y velaciclovir - y aún mismo una infección por virus JC – a pesar de la negatividad de la PCR en LCR - , dado que las alteraciones en el LCR son compatibles con una leucoencefalopatía. Si también como hipótesis aceptamos que al principio de su infección por HIV comenzó su trastorno cerebral a partir de una leucoencefalopatía multifocal progresiva (LMP) y la enferma se mantuvo viva, fue porque se le instituyó un tratamiento antirretroviral efectivo a punto tal que se normalizaron los CD4 y la carga viral cayó a 228 copias/ml. Tal mejoría de su infección por HIV también pudo haber frenado la infausta evolutividad del JC. En cambio con el tratamiento antirretroviral y antiherpético paradójicamente empeoró su estado neurológico. Es decir que con la mejoría de su VIH se está produciendo una peoría neurológica, típica conducta de un síndrome de recomposición inmune. De manera tal que de ninguna manera debe descartarse la LMP por su hallazgo negativo en el LCR. Sólo la descarta la negatividad de la PCR en una biopsia de cerebro y la ausencia de corpúsculos de inclusión en los oligodendrocitos.
CONTINÚA.
7 – La asociación del Sme. clínico imagenológico con la aparición de incontinencia urinaria y un LCR que expresa una discreta disociación albuminocitológica aboga hacia un probable Sme. de Guillain y Barre – incipiente?- que en este caso debería asociarse a la infección herpética y luego a otros microorganismos : Chlamydia pneumoniae, Campylobacter yeyuni, Micoplasmas, etcétera.
ResponderEliminar8 – Tomando en cuenta que esta paciente procede de Äfrica y apenas hace seis años está radicada en EEUU, exige considerar la modalidad linfomatosa de la infección por el virus Epstein Barr . En ese continente he tenido oportunidad de observar linfoma de Burkitt en sujetos de raza negra en regiones con alta prevalencia de infección por Plasmodium falciparum . Sin embargo el linfoma primario del SNC, como marcador cerebral en sujetos con infección por VIH, se presenta con grave inmunodeficiencia – menos de 50 CD4 – apareciendo como tumoración generalmente única ubicada a nivel de la substancia periventricular y con fuerte refuerzo del contraste . Hoy se acepta que todo linfoma primario del SNC vinculado con el SIDA contiene el genoma de virus de Epstein Barr .
CONTINÚA.
9)- Finalmente en el último LCR se observa una cantidad excesiva de hematíes en el primer tubo y ninguno en el tubo 4. Significa, casi con seguridad, un defecto de técnica mientras se ejecutaba la punción lumbar. En cambio en la primera determinación licuórica realizada 16 meses antes, la prueba de ambos tubos reveló presencia significativa de hematíes asociada con una leucocitorraquia entre 58 y 76 elementos, a predominio linfocitaria, y una proteinorraquia de 85 mg/dl. Estos hallazgos son compatibles con una encefalopatía viral .
ResponderEliminarMi cordial saludo
Olindo Martino
el caso se las trae
ResponderEliminarUna contingencia evolutiva – algunos autores la consideran complicación a distancia – a que puede llevar una leuconcefalitis, sobre todo en una mujer en edad media de la vida como el presente caso, es la Esclerosis múltiple, que si bien tiene poco al momento de describir el caso no debe ser olvidado. Lo que no sé es si se la ha descrito en sujetos VIH +
ResponderEliminarOlindo Martino
Siempre asocie el sme de reconstitucion inmune con el periodo cercano al inicio de la medicacion....gracias por recordarme que hay formas cronicas, por asi decirlo.
ResponderEliminarjimena
EXCELENTE!!!!!!!!!!!!!
ResponderEliminarFELICITACIONES Y SIGAN ASI
verdad que si el paciente es VIH positivo, el diagnostico diferencial de cualquier cosa que tenga se duplica ... muy buen caso y buenas conclusiones!
ResponderEliminarEstimado Juan
ResponderEliminarPara mí fue un interesante ejercicio que me permitió ratificar lo que estamos viendo en el Muñiz desde no hace mucho tiempo y sobre todo cuando el intenso y precoz tratamiento antiretroviral , TARGA por ej., se torna eficaz
Me refiero al Sme. de roconstitución inmune. Son las paradojas que nos depara la enfermedad rosa!
Un abrazo
Olindo
Sabino Guillermo Echebarria Mendieta
ResponderEliminarneurólogo
Hospital San Eloy ( comarca Barakaldo)
Osakidetza-Servicio Vasco de Salud
La descripción del caso da lugar a la posibilidad de realizar algunas reflexiones sobre la leucopatía /leucoencefalopatía con / sin inmunosupresión en el adulto .Los diagnósticos diferenciales a realizar vendrían dados por :
-Adulto joven con antecedente TCE leve /moderado , con rarefacción de SB y estudio realizado para descartar etiología habituales ( en este caso VIH + ) : creatincinasa , lactato , proteinograma e inmunoglobulinas , LCR , índice Ig G , autoinmunidad , serología sífilis , Salmonella , virus herpes , corticotropina , cortisol basal , aminoácidos de orina , ácidos grasos de cadena muy larga , análisis del cultivo de fibroblastos , arilsulfatasa A urinaria , ácido fitánico , cobre y ceruloplasmina , biopsia muscular y de nervio sural , biopsia cerebral.
El despistaje de afectación de SB en SIDA ( VIH -vacuolar , LMP atípica , CMV , herpes ) se recoge ampliamente en Olsen WL . White matter disease in AIDS : findings at MR imaging.Radiology 1988 ; 169: 455-488 o en Mercader JM y cols.Diagnóstico por imagen de la afectación cerebral en el SIDA .Rev Neurol 1996 .
Recientement , ante el auge del tratamiento HAART y el SRI-post HAART , se describen casos de afectación atípica de sustancia blanca , como el caso de Glez-Duarte y cols , en Neurology 2009 ; 72: 286 , describiendo formas seudo-tumorales en la conjunción VIH-JCV-SRI ( pacientes con recuento de 25 cels / -95 cels / mm3 ) pre y post HAART , con demostración de inclusiones gliales +desmielinización + astrocitos atípicos y gigantes , con diagnóstico diferencial respecto a formas de gliomatosis cerebri ( extensas cambios de señal hiperintensos en FLAIR y T2 , no objetivables en T1 o TC , con diagnóstico diferencial con el síndrome de Behcet , Sjögren , leucoencefalopatía isquémica , encefalitis infecciosas o inmunitarias , vasculitis , o CADASIL atípico
No podemos olvidar los diagnósticos diferencilaes de cuadros desmielinizantes en VIH , con series de casos recidivantes -remitentes similar al que aparece en la Esclerosis Múltiple en que el tratamiento con corticoides puede ser efectivo ( Burton BJ y cols.Steroid-responsive HIV optic neuropathy 1998 )
Más infrecuentes son las formas de presentación de las leucodistrofias en adultos ( post-TCE o episodio infeccioso/febril ) , como la myeliopathia centralis difusa ( CACH o EIF 2B ) o las leucodistrofias típicas
La verdad es que es un caso muy interesante y didáctico. Pero no me quedo claro porque este paciente hizo un síndrome de reconstitucion inmune si no tenía ninguna infeccion oportunista ni subclinica ni clinica. Yo tenia el concepto de que el sindrome de reconstitucion inmune era porque al recuperarse las defensas, una infeccion, hasta ese momento oculta o no, era rechazada o era objeto del ataque inmune endogeno.
ResponderEliminarEn este caso no hubo tal infeccion ni neoplasia. Me parecio entender que el propio virus del sida obra como antígeno?. Si es así, entonces entendi bien . De todas maneras me parece que es una perla de la medicina este articulo.
gracias
ANDRES
Estimado Juan
ResponderEliminarAdemás de apreciar sobremanera su opinión,
si Usted me lo permite desearía aclararle la duda al colega Andrés y agregar:
El concepto que debe primar en el Sme. de reconstitución inmune es el siguiente:
1- Todo proceso infeccioso en actividad, al ser desconocido por parte del hospedero, desencadena un estímulo. . Esa actividad se canaliza por la sensibilización de los linfocitos T a través de la oferta – presentación de antígenos – por parte de los macrófagos presentadores. Consecuencia: gran cantidad de producción de linfoquinas, citoquinas ( IL-3….6…etc.), FNT, etc. etc. Este fenómeno ¨ avivaría el fuego ¨ que sería lo mismo que decir reaparecería nuevamente el componente inflamatorio. Cualquier tipo de antígeno – infeccioso o no infeccioso – si tiene capacidad de estimular el sistema T dependiente posee capacidad para desencadenar inflamación.
2- Si existe un severo inmunocompromiso orgánico lo primero que se inhibe es la respuesta a la presentación de antígenos, motivo por el cual no se generará el fenómeno inflamatorio. Esa es la razón por la cual vemos un preparado histológico donde apenas muestra ante una necrosis o proceso similar con escasísimas células inflamatorias correspondiente a la fase de reactancia aguda o crónica – neutrófilos o linfomonocitos - , respectivamente.
3- Si a continuación se inicia un tratamiento antirretroviral de alta eficacia, paulatinamente es de esperar la recuperación del estado ¨ apto ¨ para crear inflamación. Esto fue lo que sucedió en esta paciente, en la cual no debemos olvidar que dentro de su organismo tenía corpúsulos virales para virus herpéticos – herpes simple 2 y Epstein Barr – y , se acepte o no, en el líquido CFR en un momento de su evolución existía antígeno capside para Epstein barr de elevado tenor. Sabemos que este virus tiene electividad para los linfocitos y ese uno de los motivos para que provoque ¨ vaivenes ¨ de actividad inflamatoria (Sme de la fatiga crónica por ej.) con silenciamiento en aquellos sujetos predispuestos.
4- Si el sistema T dependiente devuelve la capacidad inflamatoria a un organismo previamente defectuoso, cualquier estímulo - inclusive el mismo agente infeccioso viral que provoca la enfermedad de base – puede
– por principio inmunológico - simular eventualmente una reactivación de la enfermedad de base debido al resurgimiento del Sme. de reconstitución inmune. Y ello puede apreciarse en las alteraciones del último LCF presentado donde los valores son compatibles con una encefalopatía viral. Del propio virus? De otra etiología que no se ha logrado detectar? Quizás lo que más interese es que el supuesto agresor, cualquiera sea su nombre y apellido, puede emerger toda vez que la inmunidad celular reaparece.
Le saluda cordialmente
Olindo Martino
Muchas Gracias Profesor Martino por su valiosa colaboración con la página, y por compartir su rica experiencia en el campo de la Infectología durante tantos años en el Hospital "F. Muñiz", centro de referncia Argentino de Enfermedades Infecciosas.
ResponderEliminar